β细胞功能检测方法一览
检测胰岛β细胞功能方法诸多,包括胰岛素脉冲样分泌模式检测(较少用于临床研究)和胰岛β细胞分泌刺激试验(葡萄糖和非葡萄糖刺激试验)。另外还可通过分析β细胞分泌的其他肽类来判断其功能。β细胞对各种分泌刺激的反应很复杂,因而目前没有一个检测指标能完全代表β细胞功能。而且β细胞功能与胰岛素抵抗密切相关,只有校正胰岛素敏感性后,才能客观反映β细胞功能。此外还需考虑肝脏胰岛素摄取、胰岛素清除等影响血胰岛素浓度的因素。
◆ 高葡萄糖钳夹技术
高葡萄糖钳夹是经典和公认的评估β细胞功能的方法,能全面反映β细胞对葡萄糖及组织对胰岛素的敏感性。
方法简介:推注葡萄糖使血糖迅速升高至高血糖目标值,然后继续输注葡萄糖维持血糖在此目标值2~3小时,期间多点采血检测胰岛素分泌情况。
评估指标:绝对或增加的1相和2相胰岛素分泌。1相分泌(AIR)通常指8~10分钟内的胰岛素分泌,2相分泌则常用首次分泌峰衰减后的平均胰岛素水平表示,也可通过分析C肽水平获得的胰岛素分泌情况来反映β细胞功能。
点评:高糖钳夹可完整观察到胰岛素双相分泌,较精确地评价β细胞储备和分泌功能,并能同时测定葡萄糖利用,故而成为在糖尿病预测、机制研究、了解β细胞功能有关简易参数的精确性及评定药物疗效等方面的标准方法。但其结果仍受胰岛素抵抗影响,且人为导致的持续高血糖状态不符合生理模式。此外,该技术操作较复杂且费用昂贵,因而不适宜广泛的临床研究。
◆ 静脉葡萄糖耐量试验(IVGTT)
同高糖钳夹一样,IVGTT也是评价1相胰岛素分泌的经典方法。
方法简介:一次性静注葡萄糖0.3~0.5 g/kg(标准体质量),3小时内采血检测血糖和胰岛素(通常在头10分种内每隔1~2分种采血1次以评估1相分泌)。在正常人中可观察到胰岛素双相分泌。微小模型法(FSIVGTT)是在静脉推注葡萄糖后,在3~4小时收集12~30份血样,检测葡萄糖、胰岛素或C肽水平。
评估指标:最常用的是AIR,即试验开始5~10分钟内平均胰岛素增量。结合微小模型通过特定的软件可同时计算胰岛素敏感性和胰岛素分泌量。
点评:AIR是公认的较好的β细胞功能指数,在校正胰岛素敏感性后可反映2型糖尿病患者的β细胞功能受损,但不能判定晚期糖尿病患者的β细胞功能。操作相对简单,可重复性较好,但在精确性方面不如高糖钳夹,临床应用可行性仍较差。微小模型取血次数较多,适用于样本量较小的精确研究,评估的是胰岛素分泌量,而非真正β细胞功能。
◆ 稳态模型评价(HOMA)
HOMA是应用广泛的评估胰岛素抵抗和β细胞功能的研究和流调工具。这种评价方法源自基于空腹血糖和胰岛素水平的对肝脏葡萄糖输出和胰岛素分泌间平衡的数学评估方法。
方法简介:收集空腹血样,检测葡萄糖和胰岛素水平。
评估指标: HMOA β细胞功能指数(HOMA-B),其计算公式为HOMA-B=20Ib/(Gb-3.5)。
点评:这种基于空腹胰岛素检测的方法对分析的精确性有很强依赖,很小的绝对误差就可能影响计算值,同时易受胰岛素抵抗的干扰发生误判。
◆ 口服葡萄糖耐量试验(OGTT)
OGTT可评价胰岛素分泌和胰岛素敏感性,提供β细胞功能减退和2型糖尿病进展的信息。
方法简介:口服75 g葡萄糖,在0、30、60、90和120分钟时检测血糖和胰岛素水平,也可检测C肽水平。
评价指标:常用胰岛素生成指数(IGI),公式为IGI=(I30-I0)/(G30-G0)。其他经验性指数如MBCI,公式为MBCI=[FISN(空腹胰岛素)×FPG]/(PG2h+PG1h-2FPG)。OGTT还可获得空腹胰岛素(I0)、胰岛素峰值与空腹值之比(Imax/I0)、血胰岛素与葡萄糖的比值(I0/G0、I30/G30、I60/G60、I120/G120、I180/G180)、OGTT胰岛素曲线下面积。
点评:OGTT可用于糖耐量正常、空腹血糖受损、糖耐量受损个体以及2型糖尿病患者,方法简单,可广泛应用于临床。但影响因素较多(如受肠-胰岛轴受损、胰岛素抵抗的影响),血糖浓度不能标化是其缺点。此外,IGI所反映的早相胰岛素分泌以1相胰岛素分泌为主,但2相胰岛素分泌也有部分贡献,该指标不能比较胰岛素分泌曲线平坦人群的β细胞功能。
◆ C肽和胰岛素原
用C肽值评估β细胞功能常用于接受胰岛素治疗者, 因其水平不受外源性胰岛素影响。另一方面,胰岛素释放入血后一部分被肝摄取,其量不定,而C肽则甚少被肝摄取,故外周血中C肽水平较稳定,客观地反映β细胞分泌胰岛素功能。早有学者提出C肽分布、代谢动力学的二室模型,并用个体参数法计算稳态及非稳态条件下的胰岛素分泌率。在糖耐量异常者、糖尿病患者、糖尿病患者一级亲属中均可出现胰岛素原或其与胰岛素比值(PI/I)增高,故可用于评估不同糖调节状态人群的β细胞功能。
◆ 其他检测方法
胰岛淀粉样蛋白多肽(IAPP) 胰岛素分泌与IAPP相关,有学者提出假设,检测IAPP水平可预测β细胞功能障碍严重程度。但是,由于与胰岛素释放相似,IAPP在不同2型糖尿病患者中的释放也有所不同,因而在高危患者中,与评价胰岛素释放相比,评价IAPP可能并不能提供更多β细胞功能的信息。
精氨酸试验 精氨酸刺激试验是一种非葡萄糖刺激的β细胞功能试验。精氨酸刺激的胰岛素分泌强于葡萄糖刺激,即便是葡萄糖反应差的患者,精氨酸刺激后仍可有良好反应,因此可用于评价糖尿病患者残存的β细胞功能。其方法为推注5 g精氨酸后5分钟,开始收集样本检测胰岛素,计算刺激后胰岛素水平,步骤基本同IVGTT。精氨酸诱导的分泌反应与血糖水平有关,故可在不同血糖水平下多次注射精氨酸观察胰岛素分泌反应,临床主要用于观察AIR的变化。
胰高血糖素刺激试验 该试验意义同精氨酸刺激试验,常用于评估1型糖尿病胰岛β细胞功能。方法是静脉注射1 mg胰高血糖素,测定0、15、30、60和120分钟C肽或胰岛素水平。
分级葡萄糖输注试验(Graded glucose infusion test) 该法旨在试验性重建针对葡萄糖浓度的胰岛素分泌剂量反应模式,在分步持续输注葡萄糖时连续监测血糖和C肽,绘制β细胞量效曲线,获得的信息较丰富。但是,该试验持续时间较长(达6小时),也不能评估1相胰岛素分泌。受试者长期暴露于高血糖,检测结果可能有一定偏倚。
GLP-1发挥治疗性β细胞功能干预作用
胰高血糖素样肽-1(GLP-1)是重要的肠促胰素,其分泌减少与2型糖尿病密切相关。研究提示,GLP-1不仅可葡萄糖浓度依赖性降糖,而且可保护β细胞,甚至减轻体重、降低血压等。
研究显示GLP-1可刺激β细胞新生,抑制其凋亡,改善2型糖尿病患者β细胞功能,增加胰岛素分泌,改善双相胰岛素反应。
利拉鲁肽保护β细胞
利拉鲁肽(liraglutide)是1天注射1次的人GLP-1类似物,在其系列研究中,使用多种β细胞功能检测的结果已提示,其可发挥β细胞保护作用。
利拉鲁肽增加1相和2相胰岛素分泌 2006年马里(Mari)等的研究显示,利拉鲁肽可改善1相和2相胰岛素分泌,增加葡萄糖敏感性。
利拉鲁肽改善HOMA-B 德格(Degn)等对2型糖尿病患者的研究显示,利拉鲁肽可使HOMA-B改善30%。去年ADA年会发布的一项研究也显示,2型糖尿病患者在二甲双胍和(或)格列美脲治疗基础上加用利拉鲁肽治疗26周,利拉鲁肽可使HOMA-B所示β细胞功能改善28%~34%。
利拉鲁肽改善胰岛素原/胰岛素比率 研究显示,与安慰剂或罗格列酮相比,利拉鲁肽不仅可改善HOMA-B,而且可改善胰岛素原/胰岛素比率(图1)。

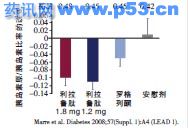
图1 检测HOMA-B和胰岛素原/胰岛素比率显示,利拉鲁肽可改善β细胞功能
利拉鲁肽可恢复β细胞的葡萄糖敏感性 常(Chang)等的研究显示,2型糖尿病患者接受单剂利拉鲁肽后,胰岛素分泌情况显著改善,β细胞对葡萄糖升高的反应性可恢复至健康对照水平。
结 语
总之,通过各种方法观察β细胞功能,可了解2型糖尿病的进展情况,并可为选择有效保护β细胞功能的治疗途径提供可靠依据。作为新一代的人GLP-1类似物,利拉鲁肽相关的采用多种β细胞功能评估方法的临床前及临床研究均显示,其具有良好的β细胞功能保护作用。而且,研究还显示利拉鲁肽具有更为重要且独特的直接增加β细胞数量的作用,此方面内容将在该专题的后续系列文章中讲解,期待读者关注。

