|
英文药名:TS-1 combination capsule T25
日文药名;ティーエスワン配合カプセルT25
中文药名;替吉奥胶囊(TS-1,S-1)
品牌药生产厂家:日本大鹏制药
药品简介
替吉奥胶囊(TS-1,S-1)是日本大鹏药品工业株式会社研制的一种复方抗癌药,是由替加氟、吉美嘧啶、奥替拉西钾组成的复方制剂,主要用于治疗不能切除的局部晚期或转移性胃癌。替加氟在体内缓慢转变为氟尿嘧啶发挥抗肿瘤作用;而吉美嘧啶能够抑制在二氢嘧啶脱氢酶作用下从替加氟释放出来的5-Fu的分解代谢,提高血浆中的5-Fu的浓度,并延长有效药物浓度的保持时间;奥替拉西可减少5-Fu对消化道粘膜的损害,抑制5-Fu的磷酸化,减少其对胃肠道的副作用。
替吉奥胶囊(TS-1,S-1)优势
替吉奥胶囊优于其他胃癌药物的显著特点在于比单纯的手术治疗更能降低胃癌患者死亡风险;能够维持较高的血药浓度并提高抗癌活性;明显减少药物毒性;给药方便等。
替吉奥胶囊说明书
【药品名称】
通俗名称:替吉奥胶囊
商品名称:国外商品名为TS-1,S-1
汉语拼音:Tiji'ao Jiaonang
英文名称:Tegafur,Gimeracil and Oteracil Potassium Capsules
【成 份】替吉奥胶囊为复方制剂,每粒胶囊含:
20mg规格:替加氟20mg,吉美嘧啶5.8mg,奥替拉西钾19.6mg。
25mg规格:替加氟25mg,吉美嘧啶7.25mg,奥替拉西钾24.5mg。
【性 状】替吉奥胶囊为硬胶囊剂,内容物为白色或类白色颗粒或粉末。
【适 用 症】替吉奥胶囊适用于不能切除的局部晚期或转移性胃癌。
【规 格】
(1)20mg (2)25mg
【用法用量】替吉奥胶囊联合顺铂用于治愈不能切除的局部晚期或转移性胃患者。
【不良反应】
一、国外临床试验:
1.联合治疗
在日本进行的以晚期胃癌患者为对象,比较替吉奥胶囊单药(连续28天口服替吉奥胶囊40-60mg/次,每日2次,休息14天)和替吉奥胶囊联合顺铂(连续21天口服替吉奥胶囊40-60mg/次,每日2次,第8天时给予60mg/m2顺铂)治疗的多中心III期随机对照试验。
非小细胞肺癌联合化疗(连续21天口服替吉奥胶囊40-60mg/次,第8天时给予60mg/m2顺铂)的晚期II期临床试验发现,可评价不良反应的55例患者均发生不良反应,
2.单药治疗
在可评估不良反应的578例患者中(不包括下述既往接受过治疗的乳腺癌、胰腺癌和胆管癌患者),不良放映发生率为87.2%(504例)。与其他类肿瘤相比既往接受过紫杉醇治疗的不能手术或复发的乳腺癌、胰腺癌和胆管癌患者的不良反应发生率较高,分别为96.4%、98.3%和94.9%。胰腺癌患者不良反应发生率较高,食欲减退、恶心、呕吐和腹泻等胃肠道反应尤为明显。
3.不良反应的发生时间和恢复时间
分析替吉奥胶囊治疗胃癌、结直肠癌、头颈癌、非小细胞肺癌(单药治疗)、不能手术或复发性乳腺癌、胰腺癌以及胆管癌晚II期临床试验入选的453例患者的不良反应发生时间,其结果如下:在整个周期中,从给药开始到白细胞计数<3000/mm³、血红蛋白<8g/dL、血小板计数<7.5×104/mm³的最低值所需时间中位值分别为27天、25天和24天;其中确认恢复至上述的标准以上者的所需时间中位值分别为7天、5.5天和6天。
与本要有关的腹泻、皮疹和口腔炎等不良反应应从首次给药开始至发生不良反应所需时间的中位值分别为24.5天、21天和28天;上述不良反应应从最严重等级到恢复正常所需时间中位值分别为9天、14天和13.5天。
4.肾功能异常患者的不良反应
国外产品上市后1年内的药品应用情况(胃癌)分析,根据性别、年龄、体重、血清肌酐值等用Cockcroft-Gault公式计算的肌酐清除率(Ccr估算值)分组,不良反应发生率随肌酐清除率下降而上升,同时不良反应严重程度升高。与首次给药采用标准剂量的患者相比,用量较低(比标准剂量低一个等级)者的不良反应发生率较低。
二、国内临床试验
结果显示,与本品有关的不良反应发生率为83.78%,其中主要为血液系统68.47%(白细胞减少发生率为45.05%,血小板减少发生率为20.72%,多为I、II度下降),消化系统46.85%(恶心、呕吐39.64%、腹泻7.21%),其他14.41%。本品的血液系统不良反应与替加氟相当,但其消化道反应明显好于替加氟。
本品相关不良事件的发生率为2.70%,主要表现为轻度的胃肠道出血、红细胞降低、发生率低于替加氟(3.48%)。
【禁 忌】
(1)对替吉奥胶囊的组成成份有严重过敏史的患者。
(2)严重骨髓抑制的患者禁用(可能会加重骨髓抑制)。
(3)重度肾功能异常的患者禁用[因5-FU分解代谢酶抑制剂-吉美嘧啶经尿排泄明显降低时可能导致5-FU的血药浓度升高从而加重骨髓抑制等不良反应。
(4)重度肝功能异常的患者禁用(可能会加重肝功能异常)。
(5)正在接受其他氟尿嘧啶类抗肿瘤药治疗(包括联合治疗)的患者禁用。
(6)正在接受氟胞嘧啶治疗的患者禁用。
(7)正在接受索立夫定及其结构类似物(溴夫定)治疗的患者禁用。
(8)妊娠或有可能妊娠的妇女禁用(详见【孕妇及哺乳期妇女用药】)
【注意事项】
慎用[下列患者应慎用替吉奥胶囊]
(1)有骨髓抑制患者[可能会加重骨髓抑制];
(2)肾功能障碍患者[因5-FU分解代谢酶抑制剂-吉美嘧啶经尿排泄明显降低时可能导致5-FU的血药浓度升高从而加重骨髓抑制等不良反应;
(3)有肝功能异常的患者[可能会加重肝功能异常];
(4)有感染性疾病的患者[感染性疾病可能会因骨髓抑制而加重];
(5)糖耐量异常的患者[可能会加重糖耐量异常];
(6)间质性肺炎或既往有间质性肺炎史的患者[可能导致症状加重或病情进展];
(7)有心脏病患者或心脏病史的患者[可能会加重症状];
(8)有消化道溃疡或出血的患者[可能会加重症状];
(9)老年患者(详见【老年用药】) 。
【孕妇及哺乳期妇女用药】
(1)妊娠或可能妊娠的妇女禁用替吉奥胶囊。
(2)哺乳期妇女服用替吉奥胶囊时应停止哺乳。
【儿童用药】低体重出生儿、新生儿、婴儿、幼儿和儿童使用替吉奥胶囊的安全性尚未得到验证。
【老年用药】由于老年人的生理功能下降,须慎重使用本药。
【药物过量】一旦发生药物过量,应密切监控,并进行支持、对症治疗。
【贮 藏】密闭,室温(10-30℃)保存。
【包装】铝塑包装。20mg规格(以替加氟计):25mg规格(以替加氟计):
【有效期】24个月
ティーエスワン配合カプセルT20/ティーエスワン配合カプセルT25/ティーエスワン配合顆粒T20/ティーエスワン配合顆粒T25
商標名
TS-1 combination capsule T20
有効成分に関する理化学的知見
テガフール
構造式

一般名
テガフール(Tegafur)
化学名
5-Fluoro-1-[(2RS)-tetrahydrofuran-2-yl]uracil
分子式
C8H9FN2O3
分子量
200.17
融点
166~171℃
性状
白色の結晶性の粉末である。メタノール又はアセトンにやや溶けやすく、水又はエタノール(95)にやや溶けにくい。希水酸化ナトリウム試液に溶ける。メタノール溶液(1→50)は旋光性を示さない。
ギメラシル
構造式

一般名
ギメラシル(Gimeracil)
化学名
5-Chloro-2,4-dihydroxypyridine
分子式
C5H4ClNO2
分子量
145.54
融点
約262℃(分解)
性状
白色の結晶性の粉末である。水酸化ナトリウム試液又はN,N-ジメチルホルムアミドにやや溶けやすく、メタノールにやや溶けにくく、エタノール(99.5)に溶けにくく、水に極めて溶けにくい。
オテラシルカリウム
構造式
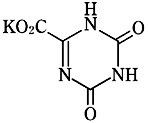
一般名
オテラシルカリウム(Oteracil Potassium)
化学名
Monopotassium 1,2,3,4-tetrahydro-2,4-dioxo-1,3,5-triazine-6-carboxylate
分子式
C4H2KN3O4
分子量
195.17
融点
300℃以上
性状
白色の結晶性の粉末である。pH8.0リン酸塩緩衝液又は水に溶けにくく、エタノール(99.5)又はメタノールにほとんど溶けない。
承認条件
1. 提出された実施計画に基づき、適切な市販後調査(特別調査及び市販後臨床試験)を実施して本剤の血液中濃度変動の要因とその程度に関する情報及び安全性等に関してデータの収集を行い、その結果を速やかに提出すること。
2. 結腸・直腸癌に対する本剤の有効性及び安全性の更なる明確化を目的とした十分なサンプルサイズを持つ無作為化比較試験を実施すること。
3. 非小細胞肺癌に対する本剤と白金含有抗悪性腫瘍剤との併用における有効性及び、安全性並びに当該併用療法の臨床的位置付けを明確にするため、非小細胞肺癌未治療例に対する標準的抗癌剤併用療法を比較対照群として、生存期間を主要評価項目とした第III相無作為化比較試験を実施すること。
包装
ティーエスワン配合カプセルT20
PTP包装:56カプセル(14カプセル×4)、84カプセル(14カプセル×6)、140カプセル(14カプセル×10)

ティーエスワン配合カプセルT25
PTP包装:56カプセル(14カプセル×4)、140カプセル(14カプセル×10)

ティーエスワン配合顆粒T20
スティック包装(0.2g):56包(28包×2)


ティーエスワン配合顆粒T25
スティック包装(0.25g):56包(28包×2)


製造販売元
大鵬薬品工業株式会社
完整处方附件:www.info.pmda.go.jp/go/pack/4229101D1025_1_03/
替吉奥胶囊临床应用研究进展
替吉奥胶囊是一种口服复方抗肿瘤药,是以替加氟为主体,加入吉美嘧啶以阻止氟尿嘧啶活化物降解,增强抗癌作用;再加入奥替拉西钾保护胃肠粘膜,减少消化道反应。三者按摩尔比为为1:0:1制成的口服胶囊制剂,用于胃癌、结肠直肠癌及头颈部肿瘤的治疗。
替加氟是5-氟尿嘧啶的前药,可在小肠吸收,具有优良的口服生物利用度和缓释能力。当替加氟进入人体后,可在肝脏线粒体P-450代谢酶系的作用下转变为5-氟尿嘧啶。
吉美嘧啶是二氢嘧啶脱氢酶的可逆竞争性抑制剂,在抑制能力上面强于尿嘧啶180倍,可允许高浓度的5-氟尿嘧啶通过代谢途径产生的代谢产物,抑制肿瘤组织中的DNA合成,以及阻断RNA功能的而发挥抗肿瘤作用。当吉美嘧啶与替加氟联用时,可在血浆中长期保持高浓度的5-氟尿嘧啶水平。在体外试验中,可观察到吉美嘧啶在人体肿瘤细胞中抑制5-氟尿嘧啶的降解,推测吉美嘧啶也可能在肿瘤中抑制二氢嘧啶脱氢酶。此外,二氢嘧啶脱氢酶的抑制可导致α-氟-β-丙氨酸聚集数量的降低,从而可以降低药物如神经毒性等方面的毒性。
奥替拉西钾本身没有抗肿瘤活性,也不作为药物单独使用。可选择性抑制胃肠道粘膜细胞中的催化酶——乳清酸磷酸核糖转移酶,从而抑制5-氟尿嘧啶磷酸化转变为5-氟尿嘧啶-5’-单磷酸酯这样一个降解过程,因此可降低胃肠道毒性的发生。动物试验中发现,在小肠中,5-氟尿嘧啶 -5’-单磷酸酯的产生与5-氟尿嘧啶进入RNA的能力降低了70%,而肿瘤组织和骨髓中的5-氟尿嘧啶 -5’-单磷酸酯只降低了0~20%。这可能是与其他组织或血浆相比,奥替拉西钾可大量的在胃肠道中聚集所导致的。奥替拉西钾可竞争性抑制乳清酸磷酸核糖转移酶,以及抑制胃肠道中5-氟尿嘧啶磷酸化转变为5-氟尿嘧啶-5’-单磷酸酯,使得胃肠道毒性大大降低。此外,氧嗪酸钾还可降低胃肠道中5-氟尿嘧啶-5’-单磷酸酯形成5-氟-2-脱氧尿苷-5’-单磷酸盐,因此可间接地维持替吉奥胶囊的活性,局部保护胃肠道,减小5 -氟尿嘧啶引起的胃肠道毒性如腹泻与排便带血等。
在日本,替吉奥胶囊于1999年被批准用来治疗晚期胃癌,2001年被批准用来治疗头颈部癌症,2003年被批准用来治疗结直肠癌,2004年被批准用来治疗非小细胞肺癌。多年的临床应用证明,替吉奥胶囊是安全有效的抗癌药物。据统计,日本目前晚期胃癌的化疗,有80%以上的病例使用替吉奥胶囊,治疗有效率可达44.6%。 日本多篇文献报道:治疗胃癌28例,有效率53.6%;替吉奥胶囊,对胃癌的有效率为46.5%。另有4篇文献报告90例,有效率38%,在单药中有较高疗效。胃癌是我国主要恶性肿瘤之一,在恶性肿瘤中占首位。每年死亡约16万人,占恶性肿瘤死亡的 23.03%。
替吉奥胶囊是替加氟及优福定的升级换代产品,其疗效明显优于替加氟、优福定和5-氟尿嘧啶。在日本已将替吉奥胶囊作为一线药物,用于治疗胃癌、头颈部癌和多种晚期转移癌等。替吉奥胶囊的优点是毒副作用小于替加氟、优福定和5-氟尿嘧啶,口服给药,方便临床患者用药。 | 









