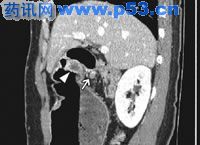
CT矢状位多平面重建示晚期胃癌
关注晚期胃癌一线化疗
今年的胃肠道癌症研讨会上,学者们交流了晚期胃癌一线治疗的研究成果。美国学者介绍了两种含顺铂化疗方案的疗效比较结果,日本学者则比较了两种以口服氟嘧啶S-1为主的方案。
顺铂联合S-1或5-FU无生存差异
来自美国M. D. 安德森(Anderson)癌症中心的阿贾尼(Ajani)等开展的多中心Ⅲ期随机临床试验表明,采用顺铂联合S-1方案(CS)或联合5-氟尿嘧啶(5-FU)方案(CF)作为晚期胃癌患者的一线治疗方法,患者生存率无显著差异。
该研究纳入了美国、欧洲和南非的1053例未经治疗的胃癌或胃食管腺癌患者,随机给予CS或CF治疗。CS方案为:第1天顺铂75 mg/m2,第1~21天S-1 25 mg/m2 bid,其后停药1周,4周为1个周期。CF方案为:第1天顺铂100 mg/m2,5-FU 1000 mg/m2连续5天输注,4周为1个周期。主要疗效终点为总生存(OS),次要终点包括总有效率(ORR)、无进展生存以及安全性。
结果显示,1029例合格患者接受化疗的中位周期数为4个。CS组中位OS期为8.6个月,CF组为7.9个月,两组患者生存情况相似,风险比(HR)为0.92(P=0.1983)。不过,CS组的安全性显著优于CF组。CS组3/4级中性粒细胞减少(18.6%对40.0%)、3/4级发热性中性粒细胞减少(1.7%对6.9%)、3/4级口炎(1.3%对13.8%)、肾脏不良事件(18.8%对33.5%)以及严重低钾血症(3.6%对10.8%)的发生率均低于CF组。另外,CS组2.5%的患者发生治疗相关性死亡,而CF组该比率为4.9%(P<0.05)。
S-1联合伊立替康或紫杉醇总有效率相似
日本国立大阪医学中心藤谷(Fujitani)等开展的Ⅱ期临床试验表明,在晚期胃癌一线治疗中,S-1联合伊立替康方案(SI)和S-1联合紫杉醇方案(SP)的ORR无显著差异。
该研究中,102例病灶大小可测量的初治局部晚期和(或)转移性胃腺癌患者随机分成SI组和SP组。SI方案具体为:S-1 80 mg/m2连续输注21天,第1天和第15天伊立替康80 mg/m2,5周为1个周期。SP方案具体为:S-1 80 mg/m2连续输注14天,第1天和第8天紫杉醇50 mg/m2,3周为1个周期。治疗持续至患者疾病进展或者发生无法耐受的毒性。研究主要终点为ORR。
两组的治疗中位周期数均为4个。SI组确定疗效持续4周以上的ORR为33.3%,SP组为32.0%。SI组最佳ORR为37.3%,SP组为36.0%。未发生治疗相关性死亡。SI组某些毒性反应以及3/4级事件较多见,如3/4级中性粒细胞减少(20.8%对2.0%)、贫血(12.5%对2.0%)、腹泻(6.3%对 2.0%)。
■ 食管癌
基因变异在胃食管反流病癌变中起重要作用
EGF基因变异增加GERD癌变危险
加拿大多伦多大学的张(Cheung)报告,表皮生长因子(EGF)基因多态性与胃食管反流病(GERD)患者的食管腺癌易感性相关,与EGF野生型A/A基因型患者相比,EGF G/G基因型者食管腺癌危险增加。
为了评价GERD是否影响EGF多态性与食管腺癌的相关性,研究者对309例食管腺癌患者和275名健康对照者的DNA样本进行了EGF基因型测定,并根据GERD病史进行分层分析。
研究者发现,与对照组相比,病例组中EGF变异(A/G或G/G)更常见(P=0.02),GERD也更普遍(P<0.001)。与EGF野生型A/A基因型相比,G/G基因型与食管腺癌危险升高相关[比值比(OR)为1.90,P=0.007]。分层分析显示,只有GERD患者亚组明显存在G/G基因型与食管腺癌的相关性(OR=3.39,P=0.005)。包括GERD症状严重性和持续时间的联合效应模型分析显示,GERD频繁发作超过1次/周或罹患GERD超过15年的G/G型患者OR最高(分别为21.8和22.4,P均<0.001)。G/G基因型和GERD之间存在高度显著的相互作用(P=0.007)。
美国西北大学芬堡医学院的欧贝尔(Obel)在点评中指出,该研究显示了GERD症状和基因如何相互作用共同增加食管癌危险。如果该研究发现获得验证,则对严重或长期GERD患者进行EGF基因型测定,有助于筛选食管腺癌高危患者。
食管腺癌挽救性切除术可行
美国M. D. Anderson癌症中心霍夫斯德特(Hofstetter)等的研究表明,根治性放化疗失败后的食管腺癌患者,仍然有希望通过挽救性食管切除术获得治疗。
有研究证实,对于以鳞状细胞癌为主的人群,在根治性放化疗后施行挽救性食管切除术是可行的。但对于食管腺癌患者,挽救性食管切除术的转归尚未明确。该研究中,45例食管腺癌患者在接受50.4 Gy的根治性放化疗失败后接受了挽救性食管切除术,研究者将这些病例资料与术前放化疗后接受择期食管切除术的300例腺癌患者资料进行了比较。
结果显示,与择期切除组相比,挽救性切除组的并发症和死亡较多。挽救性切除组吻合口瘘发生率较高(24%对9%,P=0.005),需再次重症监护者较多(18%对7% ,P=0.03),平均住院时间较长(25天对16天,P<0.02)。另外,挽救性切除组的死亡率有升高趋势(7%对3%,P=0.16)。不过,两组的5年生存率相近(47%对45%,P=0.13)。多变量回归分析提示,病理学分期、淋巴结切除数量以及年龄是生存率的独立预测因素,而挽救性策略、肿瘤部位、切除类型、吻合口瘘以及初始临床分期均不是预测因素。
因此,虽然挽救性食管切除术的短期并发症增多,但患者仍然能长期生存。这些结果提示,根治性放化疗失败和局部复发的食管腺癌患者,在有经验的中心依然可作为挽救性食管切除术的治疗对象。
Bmi-1阳性提示食管癌预后不佳
日本兵库医学院藤原(Fujiwara)等的研究表明,对于食管鳞状细胞癌患者,干细胞标志物Bmi-1表达阳性与新辅助放化疗后早期复发及预后不良相关。
Bmi-1在造血干细胞和神经干细胞的自我更新中起重要作用,是Hedgehog(Hh)信号通路的下游作用靶点。提示Hh信号转导激活的Gli-1细胞核表达可预测食管鳞癌的极早期复发,但Bmi-1在食管癌进展中的作用仍然未知。研究者通过免疫组化染色方法,分析了78例食管鳞癌患者的Bmi-1和Gli-1表达情况。
所有患者均接受术前新辅助放化疗,放疗剂量为40 Gy,化疗采用5-FU+顺铂(FP)方案。28例患者在放化疗后达病理学完全缓解。在全部患者中,24例(30.8%)Bmi-1表达阳性。所有Gli-1细胞核阳性肿瘤组织均表达Bmi-1。Bmi-1阳性患者的预后比Bmi-1阴性者显著较差,3年无疾病生存率(DFS)分别为14.9%和53.8%(P<0.005),3年总生存率(OS)分别为16.8%和56.7%(P<0.001)。
研究者认为,异常的Bmi-1信号转导激活以及Hh通路激活,可能提示新辅助放化疗后更富侵袭性的肿瘤祖细胞出现,其自身也可能成为治疗靶点。

