|
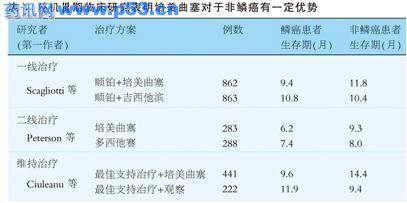
非小细胞肺癌(NSCLC)是目前发病率和死亡率较高的恶性肿瘤,其治疗也成为人们关注的焦点。近年来,随着药物的不断推陈出新、分子生物学的不断发展,肺癌的多学科综合治疗、分子靶向药物治疗以及肺癌的个体化治疗都已经取得了明显的进步,成为目前主要的研究热点。本文主要结合近年来影响NSCLC治疗的重要研究结果尤其是2009年ASCO会议上的最新进展,对NSCLC治疗的进展作一简介。 组织学类型对于制定NSCLC治疗方案越来越重要,对于细胞学或组织学标本较少的患者,可以建议做特殊染色或免疫组化帮助诊断。 较多的文献报道培美曲塞对于非鳞癌NSCLC效果较好。 TS是胸苷酸从头合成的关键酶,为 DNA合成和修复提供底物。TS表达是接受含氟脲嘧啶类药物化疗的恶性肿瘤患者的预后相关因素。近日研究聚焦于TS表达对培美曲塞疗效的预测。多数研究认为,TS低表达者腺癌较多,在小细胞肺癌中,TS表达最高。 肺癌辅助化疗 JBR.10研究:辅助化疗有生存获益 限于N1患者 随着近年来几项大规模Ⅲ期临床研究的出现,人们对辅助化疗的地位有了新的认识,术后辅助化疗的作用逐渐得到肯定。2004年加拿大NCI的JBR.10研究印证了上述结论,该研究入组482例完全切除术后ⅠB/Ⅱ期NSCLC患者,随机分为长春瑞滨+顺铂组和对照组。辅助治疗组均在手术后6周内开始辅助化疗,共4个周期。 结果显示,与对照组相比,辅助化疗组的5年生存率提高15%(69% vs. 54%,P=0.03),死亡风险降低了31%(P=0.04),化疗未导致过度的毒性反应(只有2例治疗相关性死亡事件)。 本届年会上公布了JBR.10研究的长期随访结果,统计终止日期为2008年7月,中位随访时间为9.3年,12例患者失访,271例患者死亡。生存分析表明,术后化疗可延长患者的生存(HR=0.78,95%CI 0.61~0.99,P=0.04),该获益局限于N1患者(6.8年vs. 3.6年,HR=0.68,95%CI 0.5~0.92,P=0.01),而N0患者则无显著生存获益(HR=1.03,95%CI 0.7~1.52,P=0.87)。 MSH2:可预测铂类化疗长期获益的新标志物 错配修复(MMR) 是细胞纠正复制错误的重要手段,常出现在增生过程中,以维持基因的精确性。hMLH1和hMSH2是主要的DNA错配修复控制基因,其基因的蛋白产物功能是识别和修复错配DNA.研究报道,MSH2基因蛋白产物与顺铂损伤后DNA修复相关。 本届年会上有学者报告了用免疫组化技术检测IALT研究中术后患者的MSH2表达情况,研究共对673例标本进行了分析,发现257例(38%)MSH2阳性,416例(62%)MSH2阴性。 化疗的长期生存获益在MSH2表达阳性和阴性患者中有差异,MSH2阴性患者接受化疗后生存期较对照组长(HR=0.76,95%CI 0.59~0.97,P=0.03),但是对于MSH2阳性患者,化疗未能延长生存(HR=1.12,95%CI 0.81~1.55,P=0.48)。 同时研究还发现,在658例有核苷酸错配修复交叉互补基因1(ERCC1)检测结果的患者中,随着ERCC1与MSH2阳性的个数越多,患者生存越差(P=0.01)。对于ERCC1与MSH2均为阴性的患者,接受化疗可显著延长生存(HR=0.65,95%CI 0.47~0.91,P=0.01)。MSH2可能与ERCC1一起,作为预测NSCLC铂类药物化疗长期获益的预测指标。 NATCH研究:术前或术后化疗未显著延长DFS ASCO 2009年会上报告了一项Ⅲ期临床研究(NATCH研究),研究旨在了解术前化疗或术后化疗是否较单纯手术可延长5年无病生存期(DFS)。 研究者将入组初治的Ⅰ期NSCLC患者(>2 cm)、Ⅱ期、T3N1(ⅢA期)的NSCLC患者,将其随机分为3组,一组接受单纯手术治疗,另一组接受术前3周期PC方案 化疗(紫杉醇: 200 mg/m2;,卡铂AUC=6,每3周重复) 化疗再手术,第三组患者手术后接受3个周期PC方案化疗。 研究首要目的是了解是否术前化疗或术后化疗较单纯手术可以延长5年DFS.研究共入组624例患者,其中212例患者接受单纯手术治疗,201例患者接受术前化疗,211例患者接受术后化疗。582例患者资料可用,患者中位年龄为64岁,88%为男性,50%为鳞癌,38%为腺癌,8%为大细胞癌。11%为T1N0期(>2 cm),66%为T2N0期,20.4%为Ⅱ期,2%为T3N1期。 术前化疗组中,93%的患者完成3周期化疗,缓解率为55%,6%的患者出现疾病进展;术后化疗组中,65%的患者接受了3周期的化疗。66%的患者为肺叶切除或双肺叶切除,24%的患者为全肺切除,7%的患者为开胸探查。 术前化疗组中,8%的患者出现pCR(病理完全缓解),手术组、术前化疗组和术后化疗组的5年DFS率分别为39%、40.5%和39.3%,中位DFS分别为28个月、32个月、24 个月(P=0.71)。探索性分析表明术前化疗组患者中,影像学出现缓解的患者DFS较长(62个月,P=0.09)。研究结果表明,这三组之间DFS无显著差异,等待未来数据进一步验证。 晚期NSCLC一线治疗 病理类型 病理类型影响晚期NSCLC化疗疗效的原因可能是多方面的。首先,不同的病理亚型来源于不同的胚胎组织,生物学行为可能不一致;其次,不同病理亚型的解剖定位也不完全一致(中央型或周围型),药物的浓度、药物与组织的结合、活化以及代谢均可能不一致;某些病理亚型如腺型,表皮生长因子受体(EGFR)的突变概率较高,不同病理亚型的治疗方案疗效也会出现差异。 近几年的流行病学资料表明,不同NSCLC病理组织学亚型的发生率出现明显变化,肺腺癌发病率上升速度明显快于肺鳞癌,这也会影响治疗方案的选择。我们有必要根据不同病理类型来选择治疗方案。 E4599研究:首次显示病理亚型对治疗选择的重要性 Sandler等发表在2006年《新英格兰医学杂志》的一项随机临床Ⅲ期试验(E4599研究)中,共878例晚期非鳞型NSCLC患者入组,随机分组后,分别接受一线化疗、(卡铂AUC 6,紫杉醇200 mg/m2,每3周一次,共6个周期),或联合贝伐单抗(15 mg/kg 每3周一次,持续至一年)治疗。 鉴于Ⅱ期临床研究表明,鳞癌患者用药后出血风险增加,Ⅲ期临床研究排除了出血风险较大的患者(包括鳞癌患者、脑转移患者、高血压控制不理想的患者或有出血史的患者)。 结果发现,与单纯紫杉醇/卡铂化疗比较,贝伐单抗15 mg/kg联合紫杉醇/卡铂一线治疗非鳞型晚期NSCLC,不仅可显著提高客观缓解率(35% vs. 15%,P<0.001)及延长无进展生存期(PFS,6.2个月 vs.4.5个月,P<0.001),同时也显著延长患者中位生存期(12.3个月vs.10.3个月,P=0.003)。 基于该项Ⅲ期临床研究结果,美国FDA批准贝伐单抗与紫杉醇/卡铂联合用于一线治疗无脑转移、无出血史的晚期非鳞型NSCLC.该研究首次显示了病理亚型对治疗选择的重要性。 2008年Scagliotti等报告的一项Ⅲ期临床研究,将1725例初治的ⅢB或Ⅳ期NSCLC患者随机分为2组,分别接受顺铂+吉西他滨(863例)或顺铂+培美曲塞(862例)治疗。 研究结果表明,顺铂+培美曲塞组OS不劣于顺铂+吉西他滨组(10.3个月 vs. 10.3 个月;HR = 0.94,95% CI 0.84~1.05)。但病理亚组分析表明,在腺癌患者(847例)中,顺铂+培美曲塞组患者生存期优于顺铂+吉西他滨组患者(12.6个月vs. 10.9个月),在大细胞癌患者(153例)中也得出相似结果(10.4 个月vs. 6.7个月)。而在鳞癌患者(473例)中,情况恰恰相反,顺铂+吉西他滨组患者生存期优于顺铂+培美曲塞组(10.8个月 vs. 9.4个月)。该研究是第一项显示不同病理亚型NSCLC患者生存差异的前瞻性Ⅲ期临床研究。 另有两项研究结果支持,不管是二线治疗还是维持治疗,培美曲塞对于非鳞癌较目前常药物都有一定的优势(表1)。
生物标记物 IPASS研究:EGFR突变是吉非替尼一线治疗疗效预测因素 2008年欧洲临床肿瘤学会(ESMO)年会上,Tony Mok报告了有中国学者参与的一项针对亚裔患者的开放的随机多中心Ⅲ期临床研究(IPASS研究),研究主要终点为PFS.研究共入组来自亚洲的1217例初治晚期(ⅢB或Ⅳ期)NSCLC患者,所有患者均为腺癌、非吸烟或较少吸烟(戒烟至少15年或每年吸烟量不多于10包)。大约50%的患者来自中国,20%来自日本,30%来自亚洲其他地区。 该研究将患者随机分为2组,分别给予吉非替尼或卡铂/紫杉醇方案一线治疗。研究结果表明,吉非替尼PFS较卡铂/紫杉醇有优势。 ASCO 2009年会上,Fukuoka等报告了对IPASS研究中683例患者标本进行分子生物学标志物分析的结果。该研究通过突变特异性扩增系统(ARMS)检测EGFR突变情况(60% M+)。 结果显示,EGFR 突变患者中,接受吉非替尼治疗者的PFS优于接受卡铂/紫杉醇者(HR=0.48,95% CI 0.36~0.64,P<0.0001),而EGFR野生型患者中情况正好相反(HR=2.85,95%CI 2.05~3.98,P<0.0001)。生存分析表明,EGFR 突变患者中接受吉非替尼治疗的生存时间较长(HR=0.78;95% CI 0.50~1.20),EGFR 野生型患者中接受卡铂/紫杉醇治疗者的生存时间较长(HR=1.38,95% CI 0.92~2.90)。 通过免疫荧光原位杂交(FISH)方法检测406例患者的EGFR基因拷贝数(FISH,61% FISH +)发现,不同基因拷贝数患者之间的PFS与缓解率无显著差异。同样EGFR蛋白表达与否对于PFS无显著影响。 研究者认为,EGFR突变状况是预测吉非替尼与卡铂/紫杉醇一线治疗疗效的重要因素。 FLEX研究:KRAS突变不能预测西妥昔单抗联合一线化疗疗效 ASCO 2008年会上Pirker等报告了FLEX研究结果,该研究共入组1125例EGFR阳性的晚期NSCLC患者,按1:1比例随机分为两组,A组(557例)给予NP方案(长春瑞滨+顺铂)化疗联合西妥昔单抗治疗,西妥昔单抗的起始剂量为400 mg/m2/周,第二周开始改为250 mg/m2/周;B组(568例)只接受NP方案化疗。 结果显示,西妥昔单抗组患者的中位生存期为11.3个月,1年生存率为47%,而单纯化疗组的中位生存期为10.1个月,1年生存率为42%,两组生存有显著差异(P=0.044)。西妥昔单抗组的总缓解率高于单纯化疗组(36% vs. 29%,P=0.012)。 FLEX研究是第一项证实靶向药物(EGFR抑制剂)与化疗联用可延长晚期NSCLC患者生存的临床研究。目前西妥昔单抗被2009版《美国国立综合癌症网络(NCCN)临床实践指南》推荐,作为晚期NSCLC患者的一线治疗。 ASCO 2009年会上公布了O"Byrne等对该研究中554例患者标本进行KRAS突变状况分析结果,分析发现379例患者有KRAS突变,突变与否不影响患者的OS与PFS.早期出现任何程度的痤疮样皮疹(1~3度)的患者(290例,56%)生存状况优于未出现皮疹患者(228例),中位生存期分别为15.0个月和8.8个月(HR=0.63,P<0.001)。 维持治疗 培美曲塞维持治疗Ⅲ期研究:非鳞癌一线获益后可考虑 Ciuleanu等在2008年美国《临床肿瘤学杂志》上发表的一项随机双盲Ⅲ期临床研究,将既往接受过4个周期铂类为主的两药联合化疗方案的患者按2:1的比例随机分为培美曲塞维持治疗组(441例)和安慰剂组(222例),将有临床获益的患者随机分为培美曲塞组和安慰剂组,两组均给予最佳支持治疗。 结果显示,培美曲塞维持治疗组的中位PFS较安慰剂组显著延长,除3~4度血红蛋白水平降低外,其余不良反应发生率培美曲塞组与安慰剂组相似。 本届年会上,Belani报告了该研究的最终结果,培美曲塞维持治疗组的中位生存期优于安慰剂组(HR=0.79,95% CI 0.65~0.95,P=0.012),其中生存获益主要为非鳞癌患者(PFS HR=0.47;OS HR=0.70)。研究者认为非鳞癌患者一线治疗获益后可考虑培美曲塞维持治疗。 ATLAS研究:厄洛替尼联合贝伐单抗用于维持治疗 ASCO 2009年会上Miller等报告了关于厄洛替尼维持治疗的Ⅲ期临床研究(ATLAS研究)。4周期贝伐单抗+化疗后疾病稳定的患者,随机接受贝伐单抗+厄洛替尼或贝伐单抗+安慰剂治疗直到疾病进展或出现不能耐受的毒性反应。研究主要研究终点为PFS,次要研究终点包括生存期与安全性。由于该项研究提前达到研究目的而提早终止。 结果显示,共有768例患者随机接受贝伐单抗+厄洛替尼(438例)或贝伐单抗+安慰剂(451例)治疗,其中厄洛替尼组患者的PFS明显优于安慰剂组(4.8个月vs. 3.7个月,HR= 0.722,95% CI 0.59~0.88)。 SATURN研究:厄洛替尼维持治疗改善疾病控制率 ASCO 2009年会上Cappuzzo报告了一项厄洛替尼维持治疗的随机Ⅲ期临床研究(SATURN研究)。经过4个周期化疗后疾病稳定的患者随机接受安慰剂或厄洛替尼治疗,直至疾病进展或出现不能耐受的毒性反应。 结果显示,共有889例患者随机分组,分别接受厄洛替尼治疗(438例)或安慰剂(451例),其中厄洛替尼组患者的PFS明显优于安慰剂组(HR=0.71,95% CI 0.62~0.82,P<.0001),对于免疫组化EGFR表达阳性患者,厄洛替尼组也有PFS优势(HR=0.69,95%CI 0.58~0.82,P<.0001)。厄洛替尼组缓解率为12%,安慰剂组为5%,疾病控制率分别为40.8%和27.4%(P<.0001),厄洛替尼用于维持治疗的疗效值得进一步探讨。 关于维持治疗的思考 这些最新数据进一步证实了维持治疗的有效性,但在其改变治疗规范前,尚有很多问题亟待解决。目前大部分研究中维持治疗的益处体现在PFS方面,但是仅改善PFS的意义有限,除非可同时控制肿瘤症状、减轻并发症或改善生活质量。 培美曲塞维持治疗虽然改善了OS,但对照组仅19%的患者在二线治疗时接受了培美曲塞,这就留下了不少疑问——一线治疗结束后,立即开始维持治疗,是否比同一种药物留待疾病进展后再用更好?是否需要一线治疗后给患者一段“治疗假期”?维持治疗带来的生存获益是否超过同一药物用于二线治疗?若维持治疗可带来更大的生存益处,那么获益增加与同时不良反应和治疗费用增加相比,是否值得?在未来研究给出明确解答之前,还不能说维持治疗可成为常规模式。我们同时有必要探索维持治疗的获益人群,以个体化思路为维持治疗找到出路。 ZODIAC研究:凡德他尼联合多西他赛可延长PFS Heymach等在2007年ASCO年会报道了一项Ⅱ期临床研究,结果发现关于凡德他尼联合CP方案(卡铂/紫杉醇)可延长晚期复治NSCLC患者的PFS。 本届年会上报告了一项关于凡德他尼联合多西他赛的随机Ⅲ期临床研究(ZODIAC研究)。研究入组1391例患者(平均年龄58岁,30%为女性,25%为鳞癌,10%脑转移),随机给予凡德他尼联合多西他赛(694例)或凡德他尼联合安慰剂(697例),中位随访时间为12.8个月,随访结束时87%的患者出现疾病进展,59%的患者死亡。 研究结果表明,凡德他尼联合多西他赛可显著延长PFS(HR=0.79,97.58% CI 0.70~0.90, P<0.001)与总体缓解率(17% vs. 10%,P<0.001)。研究还表明凡德他尼联合多西他赛有延长总生存的趋势(HR=0.91,97.52% CI 0.78~1.07,P=0.196)。临床资料显示,EGFR和VEGFR双通道抑制剂凡德他尼对晚期NSCLC的治疗可能具有较好的疗效和应用前景。 ZEST研究:凡德他尼与厄洛替尼对复治晚期NSCLC疗效相似 2009年ASCO 年会还报道了一项凡德他尼或厄洛替尼用于复治、晚期NSCLC的随机、双盲、Ⅲ期临床研究(ZEST研究)。研究入组1240例患者,随机接受凡德他尼(623例)或厄洛替尼(617例)治疗,中位随访时间为14月,随访结束时88%的患者出现疾病进展,67%的患者死亡。 研究结果显示,两组患者的PFS(HR=0.98,95.22 % CI 0.87~1.10,P=0.721)与生存期(HR=1.01,95.08 % CI 0.89~1.16; P=0.830)之间均无差异。但是凡德他尼治疗组腹泻(50% vs. 38%) 与高血压(16% vs. 2%)发生率较高,而厄洛替尼组皮疹发生率较高(38% vs. 28%),凡德他尼组出现3 度及以上毒性反应的比例高于厄洛替尼组(50% vs. 40%)。 ZEAL研究:凡德他尼联合培美曲塞二线治疗无额外获益 ASCO 2009年会上报告了一项凡德他尼联合培美曲塞用于晚期NSCLC二线治疗的随机双盲Ⅲ期临床研究(ZEAL研究)。研究入组534例患者(平均年龄59岁,38%为女性,21%为鳞癌,8%有脑转移),随机给予凡德他尼联合培美曲塞(256例)或安慰剂联合培美曲塞(278例)治疗。中位随访时间为9月,随访结束时83%的患者出现疾病进展,50%的患者死亡。 研究结果表明,凡德他尼联合培美曲塞未能延长PFS(HR=0.86,97.58%CI 0.69~1.06,P=0.108)与OS(HR=0.86,97.54% CI 0.65~1.13,P=0.219)。研究还表明凡德他尼联合培美曲塞组缓解率较高(19.1% vs. 7.9%,P<0.001),但是皮疹(38% vs. 26%)、腹泻(26% vs. 18%)、高血压发生率(12% vs. 3%)较高。 结 语 对于NSCLC的治疗,不论何种方法均有其适应证及局限性,因此多学科综合治疗是肺癌治疗的发展方向。同时肺癌是一种局部兼全身性的疾病,需临床医生具有不同领域的深层次知识、研究工具和仪器,涉及多学科领域,并需由多个专家参与和把握,这些更突出了肺癌多学科治疗研究的必要性和难度。很多研究证实,肺癌治疗要结合分期、类型、分子生物学才能制定较为合适、能发挥各学科最大效能的个体化治疗方案。 |
ASCO 2009年会看NSCLC治疗进展简介:
非小细胞肺癌(NSCLC)是目前发病率和死亡率较高的恶性肿瘤,其治疗也成为人们关注的焦点。近年来,随着药物的不断推陈出新、分子生物学的不断发展,肺癌的多学科综合治疗、分子靶向药物治疗以及肺癌的 ... 关键字:ASCO
2009年会看NSCLC治疗进展
责任编辑:admin
|
最新文章更多
推荐文章更多
热点文章更多 |