 |
脑胶质瘤一直是人类未能征服的肿瘤之一,被诊断为脑胶质瘤的患者就像进入了一个可怕的未知世界。虽然胶质瘤的发病率低于肺癌等其他恶性肿瘤,但其死亡率却名列前茅,给患者的家庭和社会带来了极大危害。
泰道是一种口服新型细胞毒性烷化剂,具有广谱抗肿瘤活性,可通过血脑屏障,生物利用度接近100%。循证证据证明,泰道可有效治疗新诊断及复发的胶质母细胞瘤和间变性星形细胞瘤,延长患者生存期,而且安全性和耐受性良好。泰道在中国的上市,无疑为中国脑胶质瘤患者带来了新的希望。
泰道®在世界
上市会上,加拿大Rolando Del Maestro教授和Warren Mason教授同与会者分享了泰道相关国际研究结果。
泰道同步放化疗后辅助化疗是新诊断胶质母细胞瘤患者生存的希望
2005年Stupp在《新英格兰医学杂志》上发表了一项Ⅲ期临床研究结果——对于新诊断的多形性胶质母细胞瘤(GBM)患者,在放疗基础上加用泰道,可使患者生存显著获益,但极少增加毒性反应。该研究共纳入573例新诊断的GBM患者,随机接受单纯放疗或放疗加持续每天泰道(75 mg/m2体表面积/天,每周7天)治疗,然后进行6个周期的泰道辅助化疗(150~200 mg/m2,28天为1个周期,每个周期连续5天)。主要终点为总生存情况。中位随访28个月后,泰道加放疗组患者中位生存期(OS)为14.6个月,单纯放疗组为12.1个月。泰道加放疗组2年生存率为26.5%,而单纯放疗组仅为10.4%(图1)。
泰道治疗复发性胶质瘤患者同样疗效显著
多中心临床研究比较了泰道和甲基苄肼对复发性GBM患者生存的影响。结果显示,泰道组患者6个月时无进展生存率(PFS,21%对8%,P=0.008)、总生存率(60%对44%,P=0.019)及总缓解率(45.6%对32.7%,P<0.05)均显著高于甲基苄肼组。经泰道治疗有效、复发时间在6个月以上的患者,也可以再次选用泰道治疗复发疾病。
Mason教授提出,对于放疗后复发者应注意区分疾病假性进展(放疗反应)和真性进展,一般在放疗结束3个月内难以鉴别。接受放疗+泰道治疗者比单纯放疗者更易发生假性进展,放疗+泰道治疗后最初3个月内发生的假性进展一般多于真性进展。此外,泰道也能有效治疗复发性间变星形细胞瘤和复发性间变少突胶质瘤。
大量循证证据显示,泰道是一种独特的抗肿瘤药物,对高级别胶质瘤、复发性高级别胶质瘤的疗效均优于传统化疗药物。并且,超过1000例患者的安全性研究证实,泰道安全性良好,可预测的骨髓抑制为其剂量限制性毒性反应,非血液学毒性反应轻微。
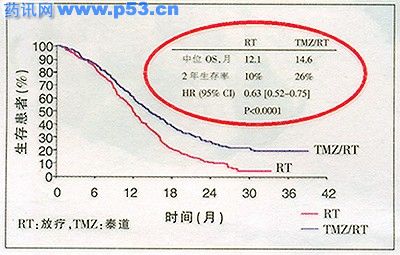 |
图1 各治疗组总体生存情况
泰道®来中国
国内注册临床研究证实:泰道治疗中国复发性GBM和AA患者同样安全有效
天津医科大学总医院杨树源教授讲述了由我国15家医院共同开展的泰道对比司莫司汀治疗复发性GBM和间变性星形细胞瘤(AA)的疗效和安全性研究。
这是一项随机开放研究,共纳入151例经常规治疗后复发的GBM和AA患者,分别接受泰道[曾接受过化疗者起始剂量为150 mg/(m2·d),未接受过化疗者起始剂量为200 mg/(m2·d),连续给药5天,每28天为1个周期)或司莫司汀[起始剂量为150 mg/(m2·d),每隔28天给药1次]治疗。评估两组患者治疗2、3和6个月的PFS和安全性。
结果显示,在意向治疗(ITT)人群中,泰道组患者6个月的PFS显著高于司莫司汀组(78.87%对55.88%,P=0.0423)。泰道组患者肿瘤缓解率和控制率也显著高于司莫司汀组(表1)。
在安全性方面,无论总不良事件还是药物相关不良事件,泰道组发生率均显著低于司莫司汀组。
该研究在中国复发性GBM和AA患者中再次证实,泰道治疗复发性GBM和AA的疗效明显优于司莫司汀——泰道组PFS和肿瘤客观缓解率均明显高于司莫司汀组,且药物安全性好。该结果与国外临床研究结果相似。
值得期待的中国临床研究
泰道在中国的临床研究计划还在不断进行,其中脑胶质瘤和实体瘤脑转移的治疗将是两个主要研究方向。
START研究是在新诊断的GBM患者中比较泰道早期(术后15~28天)化疗与术后5~10周泰道联合放疗的疗效及安全性。实体瘤脑转移的治疗和预防研究则是为了评价泰道加标准方案治疗和预防实体瘤脑转移的疗效和安全性。
国内注册临床研究证实:泰道治疗中国复发性GBM和AA患者同样安全有效
天津医科大学总医院杨树源教授讲述了由我国15家医院共同开展的泰道对比司莫司汀治疗复发性GBM和间变性星形细胞瘤(AA)的疗效和安全性研究。
这是一项随机开放研究,共纳入151例经常规治疗后复发的GBM和AA患者,分别接受泰道[曾接受过化疗者起始剂量为150 mg/(m2·d),未接受过化疗者起始剂量为200 mg/(m2·d),连续给药5天,每28天为1个周期)或司莫司汀[起始剂量为150 mg/(m2·d),每隔28天给药1次]治疗。评估两组患者治疗2、3和6个月的PFS和安全性。
结果显示,在意向治疗(ITT)人群中,泰道组患者6个月的PFS显著高于司莫司汀组(78.87%对55.88%,P=0.0423)。泰道组患者肿瘤缓解率和控制率也显著高于司莫司汀组(表1)。
在安全性方面,无论总不良事件还是药物相关不良事件,泰道组发生率均显著低于司莫司汀组。
该研究在中国复发性GBM和AA患者中再次证实,泰道治疗复发性GBM和AA的疗效明显优于司莫司汀——泰道组PFS和肿瘤客观缓解率均明显高于司莫司汀组,且药物安全性好。该结果与国外临床研究结果相似。
值得期待的中国临床研究
泰道在中国的临床研究计划还在不断进行,其中脑胶质瘤和实体瘤脑转移的治疗将是两个主要研究方向。
START研究是在新诊断的GBM患者中比较泰道早期(术后15~28天)化疗与术后5~10周泰道联合放疗的疗效及安全性。实体瘤脑转移的治疗和预防研究则是为了评价泰道加标准方案治疗和预防实体瘤脑转移的疗效和安全性。
表1 泰道组肿瘤缓解和控制率显著高于对照组

泰道研发的重要里程碑
● 1984年:Stevens 合成泰道的有效成分替莫唑胺;
● 1984-87年:动物试验证实替莫唑胺具有广谱抗肿瘤活性和低毒特性;
● 1988-91 年:英国癌症研究院下属研发企业开展Ⅰ期试验,发现替莫唑胺对人类恶性黑色素瘤和脑胶质瘤具有抗肿瘤活性;
● 1991-93 年:先灵葆雅公司获得替莫唑胺在全球的开发经营权,进一步在全球开展Ⅰ期临床试验;
● 1994-96年:开展国际多中心关键性高级别恶性胶质瘤与晚期恶性黑色素瘤Ⅱ/Ⅲ期注册临床研究;
● 1999年:欧盟 EMEA和美国 FDA 先后批准泰道上市: 治疗复发性GBM 和AA。此外,包括澳大利亚在内的 20 多个国家根据Ⅲ期临床研究结果,还批准泰道用于治疗晚期恶性黑色素瘤;
● 2005年:Ⅲ期临床研究显示,泰道联合放疗较单纯放疗显著延长新诊断 GBM 患者的无病生存和总生存。这一成就也被ASCO评为2005年肿瘤治疗领域重大进展之一。同年,FDA 和 EMEA 进一步批准泰道联合放疗用于治疗新诊断 GBM;
● 2008年:泰道在中国上市。
专家寄语
中国医学科学院肿瘤医院孙燕院士:近年来,脑胶质瘤的治疗取得了一定进展。替莫唑胺对脑肿瘤有较好疗效,所以肿瘤学界对该药寄予厚望。希望中国的同道们在使用替莫唑胺的过程中积累一些更好的经验,开展一些高水平、前瞻性临床试验,在循证医学基础上对全球肿瘤学进展做出贡献。相信泰道(替莫唑胺)会给中国肿瘤患者,尤其是脑肿瘤患者带来新希望。
上海复旦大学附属华山医院史玉泉教授:国外资料显示,替莫唑胺对脑胶质瘤疗效很好。特别是不能手术者仅用替莫唑胺化疗,也能获得较好的生存结果。而且泰道和放疗联用效果更好。因此,泰道在中国上市对广大肿瘤科和神经外科医师以及脑肿瘤患者无疑是一个福音。希望泰道在中国的临床应用取得好的效果,造福广大患者。
首都医科大学附属北京天坛医院张俊廷教授:GBM是恶性程度最高的脑肿瘤,为了巩固术后疗效,多需辅助治疗。对外科医生而言,我们不仅希望通过辅助治疗来巩固手术成果,更希望获得大量循证证据,加深对药物疗效的认识,推动医学发展。希望泰道在中国上市,能使更多脑肿瘤术后患者从中获益
。
● 1984年:Stevens 合成泰道的有效成分替莫唑胺;
● 1984-87年:动物试验证实替莫唑胺具有广谱抗肿瘤活性和低毒特性;
● 1988-91 年:英国癌症研究院下属研发企业开展Ⅰ期试验,发现替莫唑胺对人类恶性黑色素瘤和脑胶质瘤具有抗肿瘤活性;
● 1991-93 年:先灵葆雅公司获得替莫唑胺在全球的开发经营权,进一步在全球开展Ⅰ期临床试验;
● 1994-96年:开展国际多中心关键性高级别恶性胶质瘤与晚期恶性黑色素瘤Ⅱ/Ⅲ期注册临床研究;
● 1999年:欧盟 EMEA和美国 FDA 先后批准泰道上市: 治疗复发性GBM 和AA。此外,包括澳大利亚在内的 20 多个国家根据Ⅲ期临床研究结果,还批准泰道用于治疗晚期恶性黑色素瘤;
● 2005年:Ⅲ期临床研究显示,泰道联合放疗较单纯放疗显著延长新诊断 GBM 患者的无病生存和总生存。这一成就也被ASCO评为2005年肿瘤治疗领域重大进展之一。同年,FDA 和 EMEA 进一步批准泰道联合放疗用于治疗新诊断 GBM;
● 2008年:泰道在中国上市。
专家寄语
中国医学科学院肿瘤医院孙燕院士:近年来,脑胶质瘤的治疗取得了一定进展。替莫唑胺对脑肿瘤有较好疗效,所以肿瘤学界对该药寄予厚望。希望中国的同道们在使用替莫唑胺的过程中积累一些更好的经验,开展一些高水平、前瞻性临床试验,在循证医学基础上对全球肿瘤学进展做出贡献。相信泰道(替莫唑胺)会给中国肿瘤患者,尤其是脑肿瘤患者带来新希望。
上海复旦大学附属华山医院史玉泉教授:国外资料显示,替莫唑胺对脑胶质瘤疗效很好。特别是不能手术者仅用替莫唑胺化疗,也能获得较好的生存结果。而且泰道和放疗联用效果更好。因此,泰道在中国上市对广大肿瘤科和神经外科医师以及脑肿瘤患者无疑是一个福音。希望泰道在中国的临床应用取得好的效果,造福广大患者。
首都医科大学附属北京天坛医院张俊廷教授:GBM是恶性程度最高的脑肿瘤,为了巩固术后疗效,多需辅助治疗。对外科医生而言,我们不仅希望通过辅助治疗来巩固手术成果,更希望获得大量循证证据,加深对药物疗效的认识,推动医学发展。希望泰道在中国上市,能使更多脑肿瘤术后患者从中获益
| 药品价格(单位:元) | ||||||
|
编号 |
药品名称 |
通用名 |
产地 |
规格 |
单位 |
参考价 |
| 131093 | 泰道 | 替莫唑胺胶囊 | University of Iowa-College of Pharmacy | 100mg*5粒 | 盒 | 5300.00 |
| *声明:以上价格仅作参考,实际价格以药房各分店为准。 | ||||||

